Biokomplex-RiV (BK-RiV)
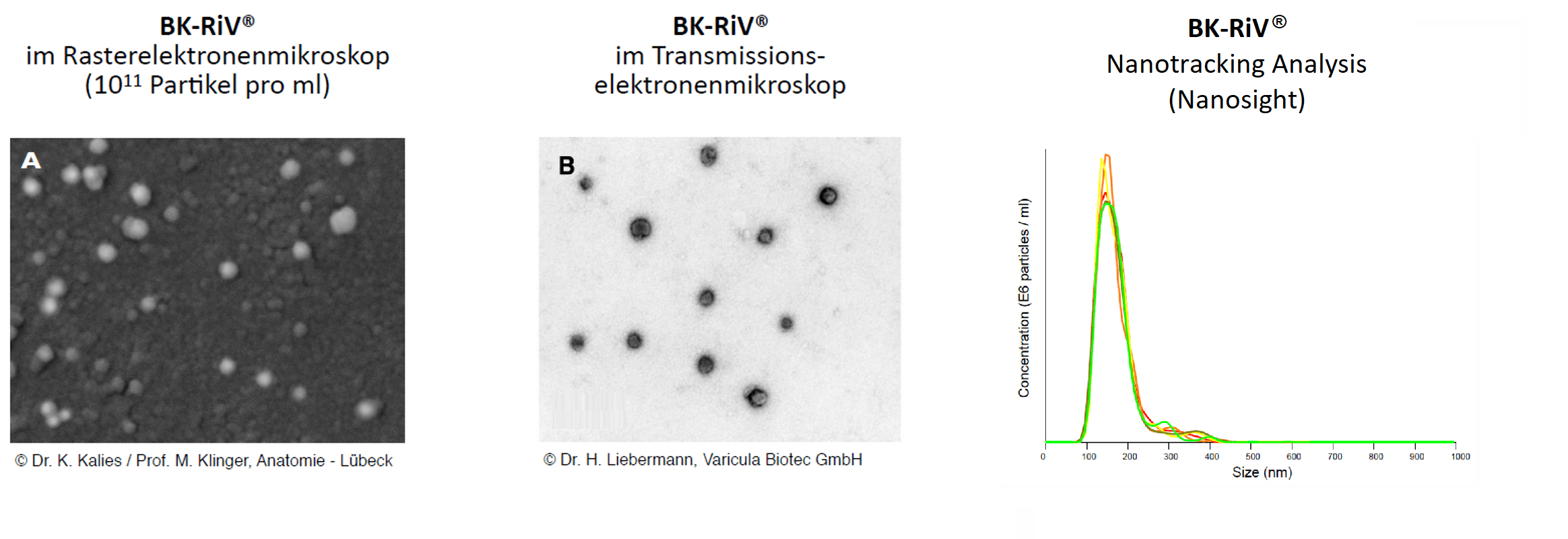
BK-RiV steht für einen partikulären Biokomplex, der im Zuge eines Reaktionsmusters in Vertebratenzellen unter bestimmten Bedingungen gebildet wird. Dieser etwa 100 nm große Biokomplex entsteht in Zellen, die einem spezifischen Stress ausgesetzt werden1 und besteht aus verschiedenen Proteinen und Nukleinsäuren2. RiV-Partikel haben vielfältige biologische Funktionen und können durch Beeinflussung des Immunsystems bei ganz unterschiedlichen Krankheiten positive Effekte erzielen1,3-7. In gereinigter isolierter Form stellen sie einen pharmakologisch aktiven Wirkstoff dar, der zur Stimulation oder Dämpfung des Immunsystems genutzt werden kann3-5,8.
Annexine
Annexine befinden sich meist innerhalb von Zellen. Erstaunlicherweise können sie aber auch extrazellulär vorkommen. Annexine können sich hochaffin an bestimmte Phospolipide (z.B. Phosphatidylserin, PS) binden, die vor allem auf der Oberfläche von Tumorzellen und virusinfizierten Zellen vorkommen9-11. So können RiV-Partikel möglicherweise Annexin-vermittelt Tumor- und virusinfizierte Zellen erreichen12,13 Es ist bekannt, dass Annexine entzündungshemmend bei beschädigten Zellen oder Geweben wirken14.
Calreticulin
CAR ist ebenfalls ein intrazelluläres Protein, dass nur unter bestimmten Umständen die Zelle verlassen kann. Außerhalb der Zelle verbessert CAR die Aufnahme sterbender Tumorzellen durch dendritische Zellen und die Präsentation der Tumorantigene. Dadurch wird der immunogene Zelltod von Tumorzellen verstärkt, d.h. das eigene Immunsystem kann sich besser gegen Tumorzellen wehren15.
Histone
BK-RiV enthält verschiedene Histone, welche normalerweise als DNA-bindende Proteine im Zellkern funktionieren. Außerhalb der Zelle setzen Histone (oder deren Spaltprodukte) Hormone frei16, verbessern die Regeneration des Knochenmarks17, verstärken den immunogenen Zelltod von Tumorzellen oder wirken anti-mikrobiell18,19.
Hitzeschockproteine
HSPs sind hochkonserviert und kommen in den Zellen der meisten lebenden Organismen vor. Dort sind sie an vielen biologischen Prozessen beteiligt. Auch HSPs wurden außerhalb der Zelle nachgewiesen. Dort wirken sie aktivierend auf wichtige Immunzellen, wie z.B. dendritische Zellen und natürliche Killerzellen. Außerdem verstärken sie den immunogenen Zelltod von Tumorzellen20.
Peroxiredoxine
Zu dieser Proteinklasse gehören Vertreter, die auch NK-cell enhancing factor genannt werden, da sie NK-Zellen stimulieren können21. Außerdem wirken Peroxiredoxine anti-viral (HIV)22 und entzündungshemmend23.
Fachkreisinformationen für Ärzte und Heilpraktiker
Aufgrund des Heilmittelwerbegesetz (HWG) sind bestimmte Informationen nur unter Auflagen zugänglich. Sie bekommen weiterführende Informationen über das DocCheck Portal.
Quellen
- Ein bisher unbekanntes Reaktionsmuster in Vertebratenzellen (RiV). 2. Mitteilung: Die Schutzwirkung von RiV-Partikel-Praparaten gegen Maul- und Klauenseuche bei Meerschweinchen.
Solisch, P. et al. (1986) Zentralbl Allg Pathol, 131, 563-568 - Use of BC-RiV pre- parations, method of production and containing proteins.
Solisch, P. et al. (1998) Patent EP 0889 053 A2 - The bio-complex “reaction pattern in vertebrate cells” reduces cytokine-induced cellular adhesion molecule mRNA expression in human endothelial cells by attenuation of NF-kappaB translocation
Rönnau, C. et al. (2009) BMB reports, 42, 106-112 - Die Autoimmunerkrankung Epidermolysis bullosa acquisita: Modulation über das adaptive Immunsystem in der Effektorphase und Beeinflussung der Wundheilung durch Protein-Nukleinsäure-Komplexe
Hauenschild, E. M. (2014) Dissertation, Institut für Anatomie, Universität zu Lübeck - Untersuchungen zur immunmodulatorischen Wirkung hoch konservierter Protein-Nuklein-Komplexe (PNACs)
Ölke, B. (2009) Diplomarbeit, Institut für Anatomie, Universität zu Lübeck - Casuistry Reports
Varicula Biotec GmbH, Teterow - Ein bisher unbekanntes Reaktionsmuster in Vertebratenzellen (RiV). 3. Mitteilung: Therapieversuche mit Hilfe von RiV-Partikelpraparaten bei Mausen mit Mammakarzinom.
Solisch, P. et al. (1987) Zentralbl Allg Pathol, 133, 293-298 - Charakterisierung der humoralen Immunantwort von C57BL/6-Mäusen nach Infektion mit Leishmania major
Kunz, N. (2013) Masterarbeit, Institut für Anatomie, Universität zu Lübeck - Elevated expression of phosphatidylserine in the outer membrane leaflet of human tumor cells and recognition by activated human blood monocytes
Utsugi, T. et al. (1991) Cancer Res, 51, 3062-3066 - Effect of X31 influenza virus fusion on phosphatidylserine asymmetry in erythrocytes
Pak, C. C. et al. (1996) Biochim Biophys Acta, 1278, 98-104 - Phosphatidylserine is a marker of tumor vasculature and a potential target for cancer imaging and therapy
Ran, S. et al. (2002) Int J Radiat Oncol Biol Phys, 54, 1479-1484 - A novel assay for apoptosis. Flow cytometric detection of phosphatidylserine expression on early apoptotic cells using fluorescein labelled Annexin V
Vermes, I. et al. (1995) J Immunol Methods, 184, 39-51 - Untersuchungen zu Interaktionen ausgewählter RiV- Proteine
Merkert, S. (2005) Bachelorarbeit, Institut für Biologie, Universität zu Lübeck - Annexin I surface binding sites and their regulation on human fibroblast-like synoviocytes
Sampey, A. V. et al. (2000) Arthritis Rheum, 43, 2537-2542 - Calreticulin exposure increases cancer immunogenicity
Clarke, C. et al. (2007) Nat Biotechnol, 25, 192-193 - Histones as extracellular messengers: effects on growth hormone secretion
Brown, O. A. et al. (1997) Cell Biol Int, 21, 787-792 - Histone H4-related osteogenic growth peptide (OGP): a novel circulating stimulator of osteoblastic activity
Bab, I. et al. (1992) Embo J, 11, 1867-1873 - Parasin I, an antimicrobial peptide derived from histone H2A in the catfish, Parasilurus asotus
Park, I. Y. et al. (1998) FEBS Lett, 437, 258-262 - Hipposin, a histone-derived antimicrobial peptide in Atlantic halibut (Hippoglossus hippoglossus L.)
Birkemo, G. A. et al. (2003) Biochim Biophys Acta, 1646, 207-215 - Extracellular heat shock proteins, cellular export vesicles, and the Stress Observation System: a form of communication during injury, infection, and cell damage. It is never known how far a controversial finding will go! Dedicated to Ferruccio Ritossa
De Maio, A. (2011) Cell Stress Chaperones, 16, 235-249 - Identification of a natural killer enhancing factor (NKEF) from human erythroid cells
Shau, H. et al. (1993) Cell Immunol, 147, 1-11 - HIV-1 antiviral activity of recombinant natural killer cell enhancing factors, NKEF-A and NKEF-B, members of the peroxiredoxin family
Geiben-Lynn, R. et al. (2003) J Biol Chem, 278, 1569-1574 - Peroxiredoxin: a central player in immune modulation
Robinson, M. W. et al. (2010) Parasite Immunol, 32, 305-313
